La hemorragia intracerebral se debe a la salida repentina de sangre hacia el parénquima cerebral, como consecuencia de una ruptura vascular. Es la forma más común del EVC hemorrágico y junto con la hemorragia subaracnoidea constituyen el 20% de los accidentes vasculares cerebrales. El evento cerebrovascular hemorrágico es el más devastador y también representa una importante causa de discapacidad y mortalidad a nivel mundial.
El 50% de los decesos ocurre durante la fase aguda, es decir, dentro de las primeras 48 horas, y en los siguientes 30 días la mortalidad va del 30% a 35%. Los sitios de hemorragia son distintos, ya que el 5% ocurre en el espacio subaracnoideo y el 15% se da dentro del parénquima cerebral. A la hemorragia que ocurre dentro del parénquima cerebral también se le puede llamar hemorragia intracerebral primaria o hematoma intraparenquimatoso.
La localización del sangrado del parénquima cerebral tiene relación con la arteria de la que proviene el sangrado, porque el 60% de los casos se presenta en regiones profundas porque se afectan las arterias lentículoestriadas y en menor proporción las arterias talámicas, el 31% por sangrado de arterias lobares, el 10% de arterias cerebelosas y el otro 10% restante se da en el tronco cerebral por los ramos perforantes de la arteria basilar. En algunas ocasiones la sangre no está totalmente contenida dentro del tejido cerebral, puede extenderse a los ventrículos cerebrales y también al espacio subaracnoideo, a esta forma también se le llama cerebromeníngea.
Un EVC sin tratamiento óptimo
La progresión del EVC hemorrágico sin tratamiento oportuno, se asocia con un mal pronóstico, es por esto que el diagnóstico precoz y el tratamiento adecuado son muy importantes para contener el daño, ya que la hemorragia tiene una rápida acumulación de sangre dentro del cerebro circundante y conduce a una lesión primaria que provoca deterioro repentino de la conciencia y disfunción neurológica muy importante, este daño primario ocurre en cuestión de minutos a horas, desde el inicio del evento, provoca la interrupción de la anatomía normal y conduce a una alta presión en el tejido cerebral local. El daño secundario se debe a la presencia y eliminación del hematoma formado (figura 1).
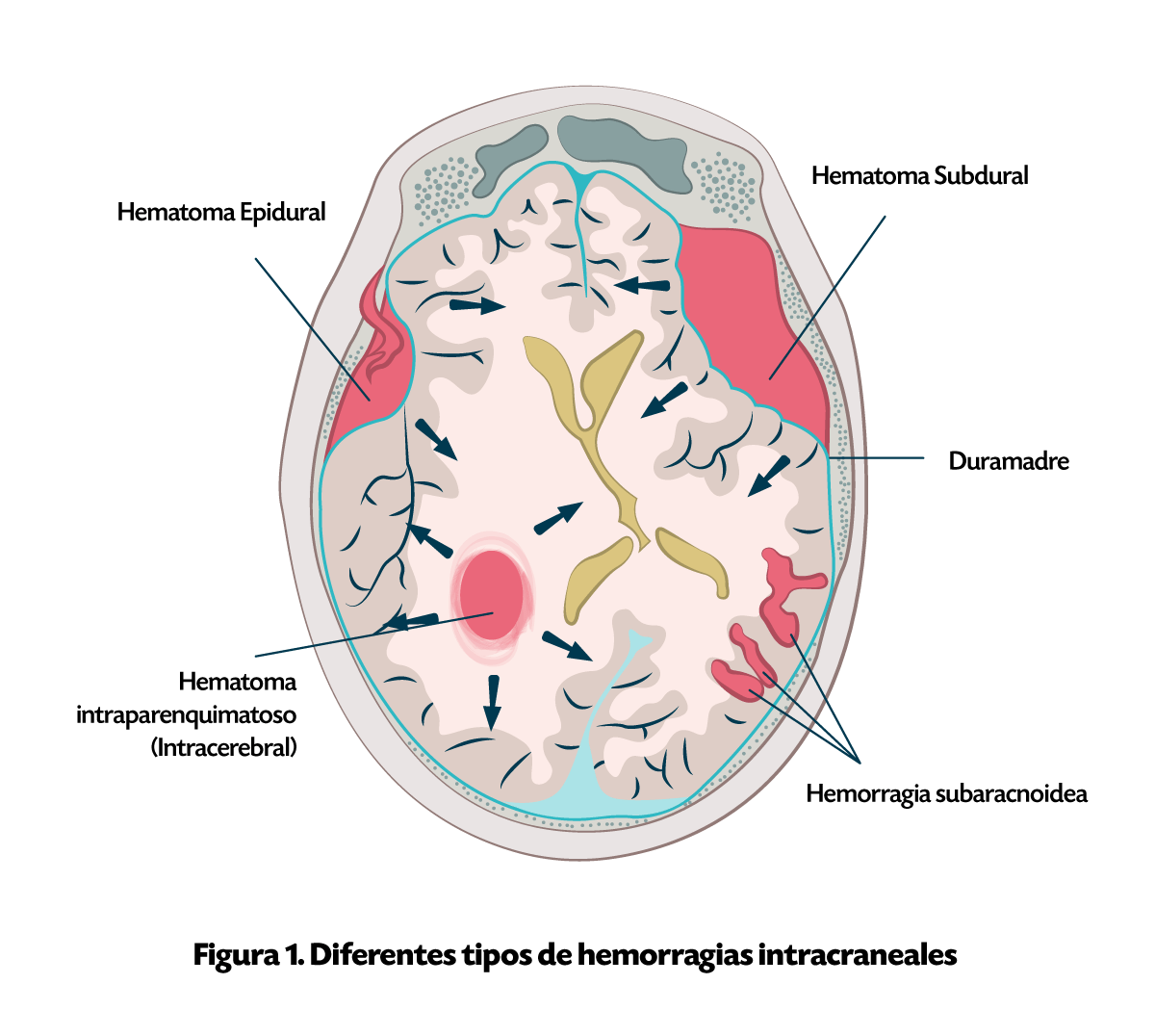
La frecuencia de la hemorragia intracerebral aumenta cuando no se trata adecuadamente la hipertensión arterial sistémica, es por lo que los enfoques actuales enfatizan el tratamiento en el control de la presión arterial en la fase aguda, revertir tempranamente los antagonistas de la vitamina K y la evacuación quirúrgica del hematoma. Aunque el tratamiento óptimo todavía se encuentra en investigación continua para poder enfrentar los retos que incluyen los cambios que se presentan después de la fase aguda.
Estudios recientes han demostrado que el sistema inmunológico innato tiene un papel muy crucial en la evolución del evento cerebrovascular hemorrágico, ya que se produce una fuerte inflamación local causada por las células inmunitarias sobre activadas, esto puede dañar gravemente o evitar la recuperación de la función neurológica después de una hemorragia intracerebral. Esto se debe a que la microglía que forma parte del sistema inmune innato residente en el cerebro se activa de una manera exagerada y luego libera citocinas y quimiocinas en respuesta al evento cerebrovascular hemorrágico que produce neuro inflamación y posterior a esto una lesión cerebral.
La microglía
La microglía es el conjunto de células del sistema inmune que se encuentran en el sistema nervioso central, también se les denomina macrófagos cerebrales. Estas células están directamente relacionadas con el desarrollo cerebral y el mantenimiento de la homeostasis neuronal, ya que dan respuesta ante las lesiones cerebrales y también participan en la reparación. La microglía se activa por varios tipos de daño cerebral y tiene la capacidad de transformarse en distintos fenotipos con funciones diferentes para mantener la homeostasis.
La microglía que se encuentra en la periferia del hematoma formado muestra un fenotipo que inhibe la inflamación, elimina el hematoma y promueve la regeneración de tejidos, se activa por los componentes sanguíneos que se encuentran en la lesión, incluidos los glóbulos rojos, leucocitos y proteínas plasmáticas, al activarse se agranda en forma de varilla o esfera fagocítica y su principal función es fagocitar el hematoma para promover la reparación del tejido cerebral y la recuperación neurológica.
Una vez activada también produce una respuesta inflamatoria aguda, estrés oxidativo, excitotoxicidad, citotoxicidad y expresa una familia de receptores similares a NOD (nucleotide binding oligomerization domain ), del dominio pirina que contiene inflamasomas NLRP3(family CARD domain containing ) que son liberados y se cree que es el principal contribuyente de la neuroinflamación (Figura 2).
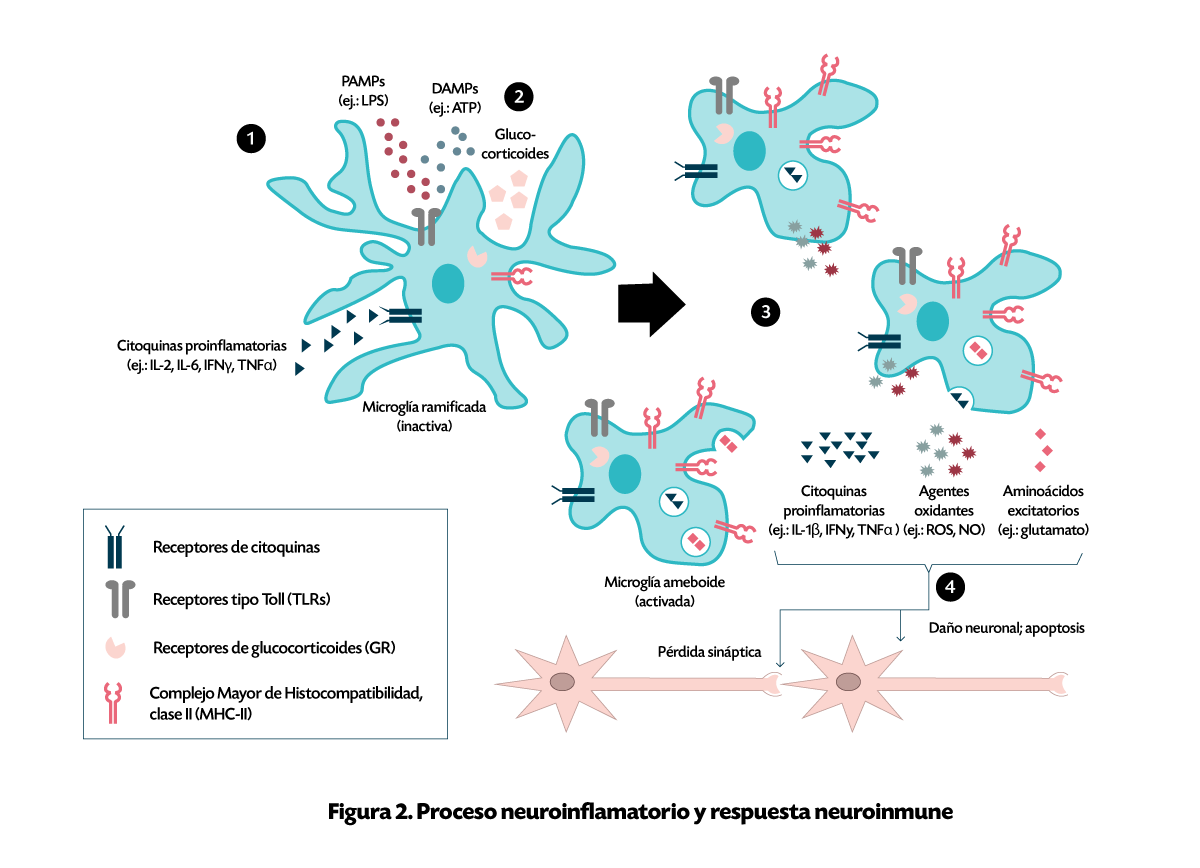
Los inflamosomas en el EVC
Los inflamosomas son conjuntos de proteínas que se encuentran en el citoplasma de las células, y actúan como sensores y mediadores del desarrollo de la inflamación. Existen diferentes clases de inflamosomas, sin embargo, todos tienen una función dirigida al reconocimiento de patógenos. Los inflamosomas se dividen en 4 categorías y se les conoce como receptores tipo Toll (TLRs), receptores tipo RIG-I (retinoic acid-Inducible gene), receptores de carbohidratos tipo lectina (CLRs) y los receptores tipo NOD (nucleotide-binding oligomerization domain). Estos últimos NOD son un grupo especializado para detectar patógenos e iniciar la respuesta inmune innata.
La familia de los NLRP, responde a señales exógenas que provienen de organismos patógenos como bacterias, hongos o virus que contengan PAMPs (pathogen-associated molecular patterns), o a señales endógenas que son moléculas conocidas como DAMPs (damage-associated molecular patterns), estas señales son liberadas por las células dañadas que se encuentran en el hematoma.
El inflamosoma más estudiado hasta la fecha es el NLRP3, también conocido como criopirina. Este inflamosoma está formado por la proteína NLRP3, la proteína adaptadora ASC (apoptosis-associated speck-like protein) y una procaspasa.
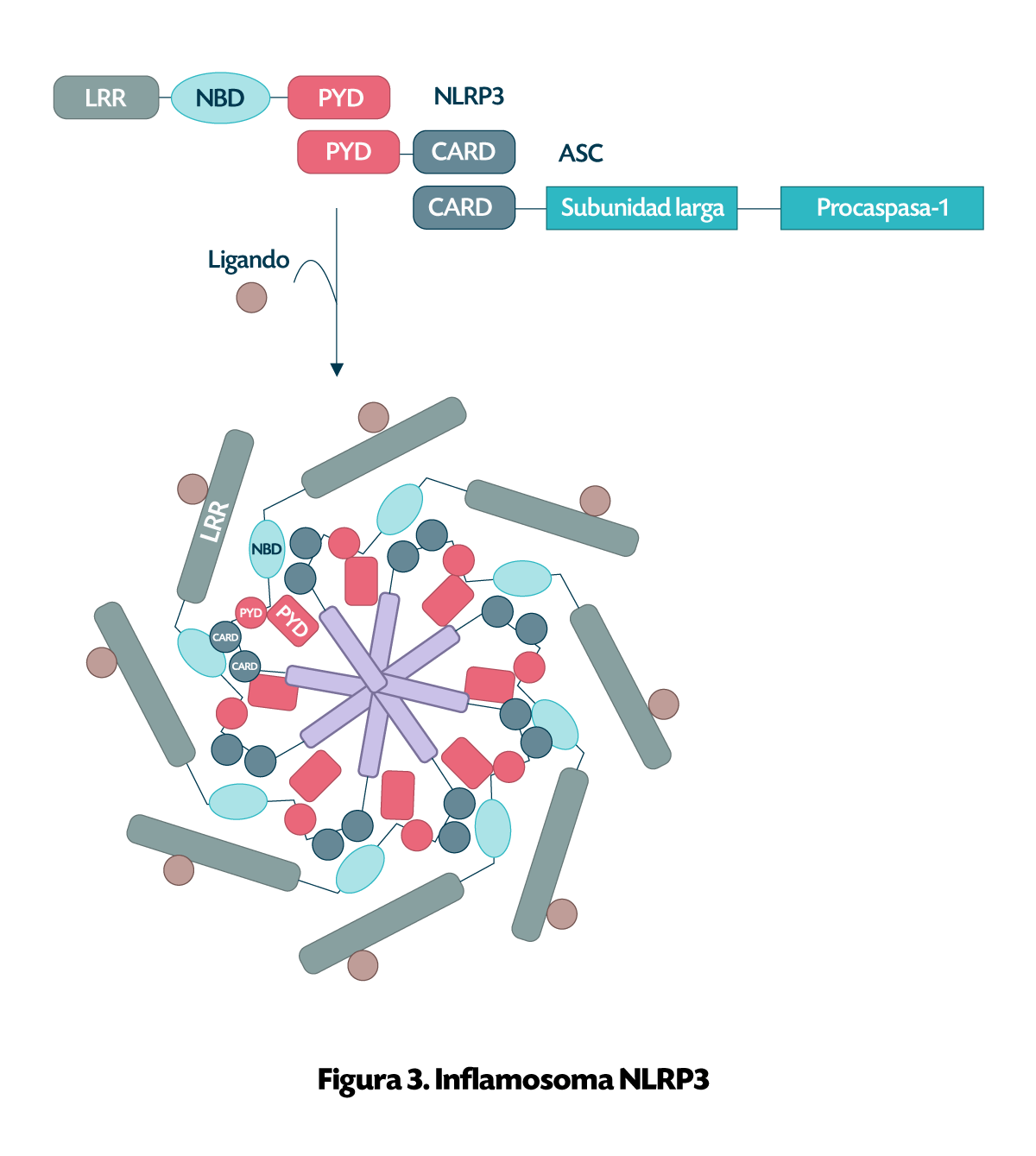
El inflamosoma NLRP3 se encuentra principalmente en los macrófagos, monocitos, células dendríticas y neutrófilos, y su principal función es combatir infecciones, pero en el proceso también puede empeorar el cuadro clínico si se activa de manera no controlada.
Varios estudios se han centrado en el papel del inflamasoma NLRP3 y en el daño cerebral provocado por el accidente cerebrovascular hemorrágico, sin embargo, el mecanismo específico de activación y regulación de NLRP3 sigue sin estar claro.
La proporción de los distintos fenotipos de la microglía determina la progresión del daño después de la hemorragia intracerebral. Por lo tanto, el estudio y manejo de la microglía puede ser un objetivo terapéutico prometedor para la hemorragia intracerebral.
Bibliografía
Ajaya Kumar A. Unnithan, P. M. (2022). Hemorrhagic Stroke. StatPearls.
Angel Miguel Santos Martinez, H. V. (2016). Hemorragia Cerebral . Invest Medicoquir , 241-262.
ArturoMontaño, D. F. (2021). Chapter 13 – Hemorrhagic stroke. Handbook of Clinical Neurology, 229-248.
L.F. Montaño Estrada, T. F. (2017). ¿Qué son los inflamosomas? . Revista de la Facultad de Medicina de la UNAM , 42-49.
Yujie Luo, C. R. (2019). NLRP3 Inflammasome in the Pathophysiology of Hemorrhagic Stroke: A Review. Current Neuropharmacology, 582-589.
Zhen Zhang, Z. Z. (2017). Microglial Polarization and Inflammatory Mediators After Intracerebral Hemorrhage. Mol Neurobiol, 1874-1886.








