Actualmente, no existe un tratamiento específico contra el nuevo virus SARS-CoV2, por lo que es importante utilizar fármacos ya existentes diseñados para virus similares, debido a que se ha probado su efectividad y cuentan con la autorización de entidades reguladoras pudiendo así combatir la enfermedad COVID-19
Debido a la situación actual se realizó un ensayo estándar para medir los efectos de cinco fármacos, entre ellos el Favipiravir, para evaluar la citotoxicidad, el aclaramiento del virus y las tasas de infección del SARS-CoV-2.
La citotoxicidad se determinó en los diferentes medicamentos al infectar las células Vero que fueron infectadas con el virus SARS-CoV-2. La eficacia se evaluó mediante la cuantificación del número de copias virales en el sobrenadante celular mediante RT-PCR cuantitativa en tiempo real y se confirmó con la visualización de la expresión de nucleoproteínas (NP) del virus mediante microscopía de inmunofluorescencia a las 48hrs posteriores a la infección.
Para Favipiravir la concentración efectiva media máxima (EC 50) fue de 61,88 μM, la concentración media citotóxica (CC 50) fue > 400 μM. El índice de selectividad (SI) fue de > 6,46, estas concentraciones fueron necesarias para reducir la infección viral con lo que se concluyó que se recomiendan más estudios in vivo para evaluar este nucleósido antiviral.1
Inicialmente el Favipiravir fue seleccionado mediante la actividad in vitro del virus de la influenza, que fue descubierto mediante la modificación química de un análogo de pirazina que es un potente inhibidor selectivo de la polimerasa del ARN viral de la influenza y ha demostrado actividad antiviral contra otros virus de ARN, haciendo a Favipiravir un fármaco prometedor para el tratamiento de las infecciones causadas por virus de ARN. 2-3
Mecanismo de acción del Avifavir (Favipiravir)
El Favipiravir Inhibe de forma selectiva y potente la ARN polimerasa dependiente de ARN (RdRp) que es una proteína esencial codificada en los genomas de todos los virus que contienen ARN, incluido el SARS-CoV-2, llevando a cabo reacciones de fosforribosilación y fosforilación adicional intracelularmente para convertirse en Favipiravir ribofuranosil-5′-trifosfato (Favipiravir-RTP).
El Favipiravir-RTP activo actúa como un terminador de elongación de la cadena de ARN naciente al competir con los nucleósidos de purina por la unión de RdRp. 4- 5
Este medicamento es un potente fármaco antivírico autorizado en Japón en 2014 para nuevas cepas de influenza, siendo objeto de estudio en el que se expusieron células infectadas por influenza a Favipiravir en diferentes momentos durante el ciclo de replicación del virus. Cuando se añadió el fármaco durante la etapa de replicación viral (0–2, 2–4 o 4–6 horas después de la infección) se observó que Favipiravir interfiere con la replicación viral. 2
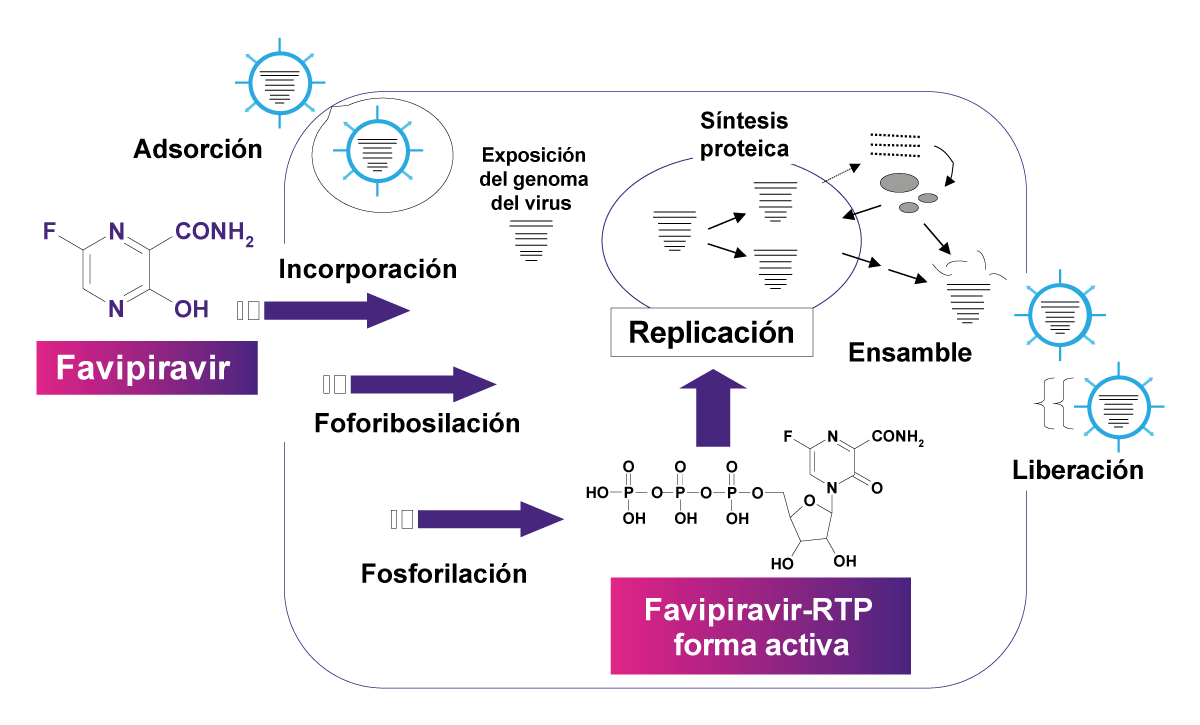
Figura 2. Mecanismo de reacción de Favipiravir
Efecto de Avifavir (Favipiravir)
Se ha evaluado su eficacia in vivo e in vitro en otras enfermedades virales como: Ébola, en la cual Favipiravir suprimió la replicación de Zaire EBOV en cultivo celular en 4 unidades logarítmicas con un Intervalo de Confianza 90% de 110 μM. Para este estudio se utilizaron ratones que carecían del receptor de interferón de tipo I como modelo in vivo para la enfermedad inducida por Ébola de Zaire. La administración de Favipiravir se realizó al día 6 después de la infección induciendo una rápida eliminación del virus, mejorando los parámetros bioquímicos de la gravedad de la enfermedad y evitó un resultado letal en el 100% de los animales. 6
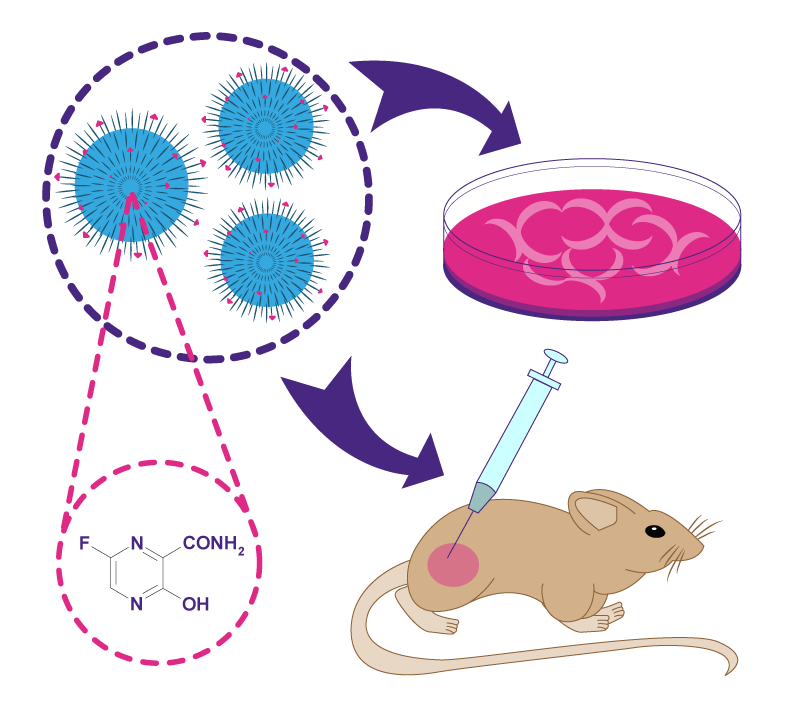
Figura 3. Ejemplificación de modelo in vivo e in vitro
Por otra parte, en un reporte de serie de casos se evaluó la tolerabilidad de Favipiravir en cuatro pacientes críticamente enfermos con COVID-19, a estos pacientes se les administró una dosis de 1600 mg dos veces al día el día 1 seguido de 600 mg dos veces al día durante 6 días (7 días en total), todos los pacientes tenían neumonía bilateral por SARS‐CoV‐2 con síndrome de dificultad respiratoria aguda. Todos los pacientes tuvieron un recuento de linfocitos en aumento durante el curso de la terapia Favipiravir, excepto un paciente que falleció debido a un choque séptico y falla multiorgánica debido a que presentaba elevación de transaminasas antes de la administración de Favipiravir y niveles de bilirrubina en aumento progresivo.
No se observó ningún otro efecto secundario posible de Favipiravir en otros pacientes. Se concluyó que la terapia de Favipiravir en dosis bajas fue bien tolerada en los cuatro pacientes críticamente enfermos. 7
En otro estudio de ensayo clínico controlado abierto para examinar los efectos de Favipiravir (FPV) versus lopinavir (LPV) / ritonavir (RTV) para el tratamiento de COVID-19, en sujetos confirmados con la enfermedad que recibieron FPV oral (Día 1: 1600 mg dos veces al día; Días 2-14: 600 mg dos veces al día) más interferón (IFN-α) por inhalación de aerosol (5 millones de unidades internacionales (UI) dos veces diariamente) se incluyeron en el brazo de FPV de este estudio, mientras que los pacientes que fueron tratados con LPV / RTV (Días 1-14: 400 mg / 100 mg dos veces al día) más IFN-α por inhalación de aerosol (5 millones de UI dos veces al día) se incluyeron en el brazo de control. Se compararon los cambios en la tomografía computarizada (TC) de tórax, el aclaramiento viral y la seguridad de los medicamentos entre los dos grupos. Se encontró una mediana de tiempo de eliminación viral más corta (7días) para el grupo de FPV frente al grupo de control. El brazo de FPV también mostró una mejora significativa en la TC de tórax en comparación con el brazo de control, con una tasa de mejora de 28.8% (P = 0,004). La mediana del tiempo hasta el cese de la diseminación viral fue de 5 días (IC del 95%: 4 días, 7 días) versus 7 días (IC del 95%: 5 días, 8 días), p = 0,129, y la mediana del tiempo hasta la curación clínica fue de 3 días. (IC del 95%: 3 días, 4 días) versus 5 días (IC del 95%: 4 días, 6 días), p= 0,03, para Favipiravir y control, respectivamente. Se observaron eventos adversos en el 36% de Favipiravir y el 8% de los pacientes de control. Un paciente de control murió debido al empeoramiento de la enfermedad. La mejora significativa en el tiempo hasta la curación clínica sugiere que el Favipiravir podría ser beneficioso en el COVID-19 leve a moderado. En el análisis multivariado con regresión de Cox mostró que el FPV se asoció de forma independiente con una eliminación viral más rápida. Además, se encontraron menos eventos adversos en el brazo de FPV que en el brazo de control. Está información sustenta el realizar investigaciones que permitan confirmar con resultados clínicos estos datos preliminares sobre el aclaramiento viral y cambios en la tomografía a favor del tratamiento con Favipiravir. 8
Otro ensayo clínico aleatorizado que reclutó a 240 pacientes con COVID-19 en el que 120 pacientes recibieron FPV (entre ellos, 116 fueron evaluados) y 120 recibieron umifenovir. El FPV se dosificó a 3200 mg el primer día, seguido de 1200 mg / día durante 10 días. Entre los pacientes con COVID-19, FPV en comparación con umifenovir, no mejoró significativamente la tasa de recuperación clínica en el día 7 (grupo FPV (71/116) versus grupo umifenovir (62/120)). Sin embargo, FPV mejoró significativamente la duración de fiebre y la tos. 9
En Rusia Favipiravir cuenta con número de registro sanitario JIII-006225 para uso en pacientes con COVID-19 bajo el nombre de AVIFAVIR*.
Efectos adversos y toxicidad
Favipiravir es tolerado razonablemente bien en los estudios clínicos, aunque se asocia con aumentos asintomáticos de los niveles séricos de ácido úrico y debe utilizarse con precaución en pacientes con gota o antecedentes de gota y en aquellos con hiperuricemia. En un estudio realizado en pacientes hospitalizados se reportaron 144 eventos adversos en los 82 sujetos de seguimiento para seguridad, el evento más frecuente reportado fue hiperuricemia en 84.1% de los sujetos, en el 11% de los sujetos se reportó elevación de triglicéridos, y en 8.5% elevación de alanino aminotransferasa sérica.10
En otro estudio realizado en pacientes hospitalizados con COVID-19 moderado, se encontró que el 17.5 % presentaron eventos adversos al medicamento, incluyendo diarrea, náuseas, vómitos, dolor de pecho y aumento de los niveles de transaminasas hepáticas. Las reacciones adversas al fármaco fueron de leves a moderadas y provocaron la suspensión temprana del fármaco en estudio en 5,0% de los pacientes.11
Estos datos sugieren que el tratamiento con Favipiravir tiene una adecuada tolerabilidad y presencia de eventos adversos no graves en los sujetos de estudio. 9
Respecto a la toxicología no clínica de Favipiravir es bien tolerado en todas las especies animales.
Los principales hallazgos de seguridad incluyen efectos adversos relevantes en seguridad humana en aspectos de reproducción y es gestionado por consentimiento informado y requisitos de anticoncepción de etiqueta hasta 3 meses después del cese del tratamiento.
De acuerdo con la hepatotoxicidad, la farmacovigilancia indica que la incidencia de reacciones adversas hepáticas suele ser asintomáticas de naturaleza transitoria y gravedad leve. Por lo general este tipo de reacciones se resuelven por si solas siendo de escasa preocupación clínica.12
Cabe mencionar que en México se iniciaron estudios con Avifavir (Figura 5).