La farmacovigilancia en la actualidad, ha tenido que adaptarse de manera rápida junto con los avances médicos y científicos para la detección, evaluación y prevención de posibles problemas ocasionados por nuevos tipos de terapias, vacunas, dispositivos médicos y productos biológicos que están en desarrollo o en etapas posteriores.
Para garantizar la seguridad de los pacientes, la farmacovigilancia se regula por las guías establecidas por los sistemas de salud local, regional e internacional (Figura 1).
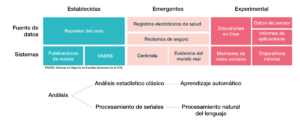
Figura 1. Descripción de las diversas metodologías de farmacovigilancia en las diferentes etapas de desarrollo.
Actualmente, la medicina de precisión es posible debido a la implementación de terapias innovadoras con el genoma humano y el sistema inmunológico, logrando así potencializar la cura de enfermedades que antes se creía que no podrían tener alcance con la medicina convencional.
Debido a esto, la farmacovigilancia ha tenido cambios acelerados, preocupados en la confiabilidad y seguridad de estas nuevas tecnologías, para actualizar las directrices de los diversos procedimientos que dan esperanza a millones de pacientes, evaluando el riesgo-beneficio que conlleva.
Nuevos modelos de tratamientos
Entre las diversas terapias se encuentra:
- Terapia génica: proporciona beneficios a través de mecanismos de acción permanente o acción prolongada. De manera similar, las terapias con células CAR-T solo están aprobadas en Estados Unidos a través de una evaluación de riesgos y mitigación, donde es importante determinar los problemas de seguridad para que puedan ser implementadas de manera general.
Consulta el artículo de Células T modificadas (CAR-T)
- Vacunas y sus respectivas formulaciones con tecnología innovadora: son otro aspecto donde los perfiles de seguridad de farmacovigilancia deberán tener nuevas adaptaciones, incluida la gestión de riesgos, ya que al compararse con las vacunas convencionales cambian los perfiles de seguridad que ya se tenían establecidos y por ende las posibles reacciones adversas que se tenían identificadas.
Un claro ejemplo es la pandemia actual, donde se destaca una situación con la farmacovigilancia posterior a la comercialización. De esta manera, se garantiza la seguridad de los pacientes en periodos prolongados, además se cumplen los estándares legislativos y prácticas adecuadas que ayudan a regular nuevas implementaciones tecnológicas en la salud y así se obtenga mayor confianza.
Legislación farmacéutica
La legislación farmacéutica proporciona y garantiza, dentro del marco legal, el uso seguro de los medicamentos que deben estar regulados por las autoridades nacionales. Además, se establecen los sistemas de farmacovigilancia para que se efectúen los compromisos regulatorios entre las diferentes partes interesadas, incluidos para su comercialización.
Éstos sistemas puedan detectar, evaluar, comprender y prevenir los efectos adversos o problemas relacionados.

Ante esta situación, la OMS apoya las vacunas y los avances tecnológicos desde el desarrollo temprano hasta la publicación de las recomendaciones políticas globales.
Una parte clave para llevar a cabo la iniciativa con capacitación y experiencia en medicina clínica es la colaboración con agencias regulatorias, academias e industrias farmacéuticas, porque su experiencia médica y científica es esencial para su transformación, debido a que la seguridad de los pacientes es una preocupación en los sistemas de salud mundial.








