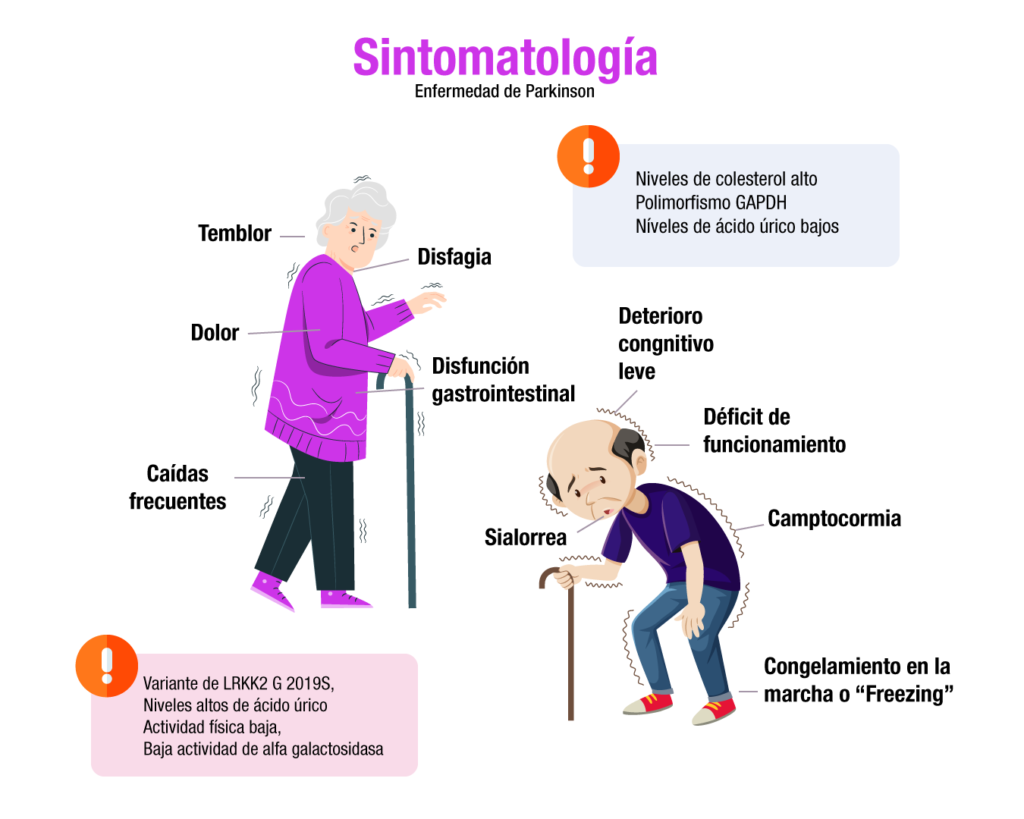
¿Cómo se dio a conocer esta enfermedad?
James Parkinson fue un pionero de la neurología clínica, nació el 11 de abril de 1755 en el distrito de Hoxton, Londres. El trabajo titulado “Ensayo sobre la parálisis temblorosa”, publicado en 1817, es un texto de 66 páginas dividido en cinco capítulos en los que se define la condición y sus características patognomónicas, el diagnóstico diferencial, la etiología y el tratamiento.
Se basa en su experiencia con seis pacientes durante varios años. El título epónimo para esta condición se le dio en 1860 propuesto por Jean-Martin Charcot, quien propuso el nombre “la maladie de Parkinson”.
La primera autopsia realizada a un paciente con enfermedad de Parkinson se realizó en 1861. En su ensayo destacó el gran impacto de esta enfermedad en los pacientes, que describió de la siguiente manera:
“El infeliz que sufre lo ha considerado un mal, del cual no tenía perspectivas de escapar de la dominación”
La notable definición que hizo de la enfermedad difiere de la definición actual con la inclusión de síntomas no motores como parte del cuadro clínico:
“Movimiento con temblor involuntario, disminución de la fuerza muscular, en partes del cuerpo que no están en movimiento e incluso cuando están apoyadas; con una postura donde se observa el tronco hacia adelante y el caminar con un ritmo de carrera: los sentidos y el intelecto están ilesos”.1
La enfermedad de Parkinson (EP) es el segundo trastorno neurodegenerativo más común después de la enfermedad de Alzheimer.2 Aunque la mayoría de los pacientes son manejados por neurólogos, la EP se presenta inicialmente al médico de atención primaria, quien debería poder realizar el diagnóstico, que se basa en la historia y el examen físico.2
El término “parkinsonismo” se refiere a un síndrome clínico, que incluye bradicinesia, rigidez de la rueda dentada, temblor en reposo, marcha lenta y desequilibrio. La causa más común de parkinsonismo es la EP, pero existe un diagnóstico diferencial prolongado y el desafío es determinar si el paciente tiene EP u otra causa de parkinsonismo, como el síndrome inducido por fármacos o parkinsoniano, como la atrofia multisistémica (MSA, anteriormente Síndrome de Shy-Drager).2
La EP se caracteriza patológicamente por la degeneración de neuronas dopaminérgicas en la sustancia negra del mesencéfalo, lo que lleva a cambios fisiopatológicos en los circuitos de los ganglios basales. Los cuerpos de Lewy es el sello citológico de la EP y contiene a-sinucleína mal plegada, la misma proteína que también se acumula en trastornos relacionados, incluida la atrofia multisistémica y la demencia con cuerpos de Lewy, denominadas colectivamente “sinucleinopatías”.2
Aunque un pequeño porcentaje de pacientes con EP tiene una causa monogenética, ya sea dominante o hereditaria recesivamente (como los genes LRRK2 o parkin, entre otros) la mayoría de los casos son esporádicos y de causa desconocida.2
La enfermedad de Parkinson suele ser asimétrica y responde al tratamiento dopaminérgico, sin indicios de antecedentes o exámenes que sugieran una causa de los síntomas. Los hallazgos patológicos muestran que las neuronas dopaminérgicas de la sustancia negra están muy disminuidas y los cuerpos de Lewy están presentes en las neuronas restantes.3
Para el diagnóstico de la Enfermedad de Parkinson2,4
Paso 1: establecer la presencia de parkinsonismo
- Bradicinesia plus
- Temblor en reposo
- Rigidez
Paso 2: identificar las características que respaldan el diagnóstico de la EP
- Respuesta inequívoca a la levodopa
- Presencia de temblor en reposo
- Pérdida olfativa
- Otros
Paso 3: no debe haber ningún criterio de exclusión absoluto
- Signos cerebelosos
- Oftalmoplejía vertical supranuclear
- Tratamiento del bloqueador del receptor de dopamina durante el último año
- Signos sensoriales corticales (agrafestesia, astereognosis)
- Imagen funcional normal del receptor de dopamina presináptico
- Otros
Paso 4: Señales de alerta que pongan en duda el diagnóstico de la enfermedad de Parkinson
- Progresión rápida (uso de una silla de ruedas dentro de los 5 años posteriores a la aparición de los síntomas)
- Caídas tempranas
- Disartria y disfagia tempranas y graves
- Fallo autonómico temprano
- Parkinsonismo bilateral simétrico
- Ausencia de algunas de las características no motoras esperadas con la EP: RBD, hiposmia, estreñimiento, ansiedad, depresión
Actualmente, una de las limitaciones importantes en el tratamiento de la EP es la detección tardía. A pesar de los rigurosos esfuerzos en el manejo del paciente y la investigación clínica, los métodos son subóptimos en las áreas de diagnóstico.5
Por lo tanto, la necesidad de biomarcadores validados con un alto grado de sensibilidad y especificidad es la necesidad del momento con el objetivo intuitivo de ayudar a diagnosticar la enfermedad.5
Un biomarcador da una indicación del estado de enfermedad particular de un organismo y evalúa el progreso de la enfermedad y los efectos del tratamiento. Puede ser un parámetro físico, químico o biológico.5
En el diagnóstico de la EP, aunque no se han recomendado biomarcadores individuales, pueden combinarse racionalmente para predecir el estado y la progresión de la enfermedad. Las dificultades para diagnosticar la EP dificultan la búsqueda de biomarcadores, ya que identificar los criterios diagnósticos de una enfermedad es importante para identificar y validar los biomarcadores. Aunque los biomarcadores de la EP son diversos (tabla1), se pueden dividir en tres etapas: la EP prodrómica, preclínica y clínica.5
Tabla 1. Biomarcadores en la EP5
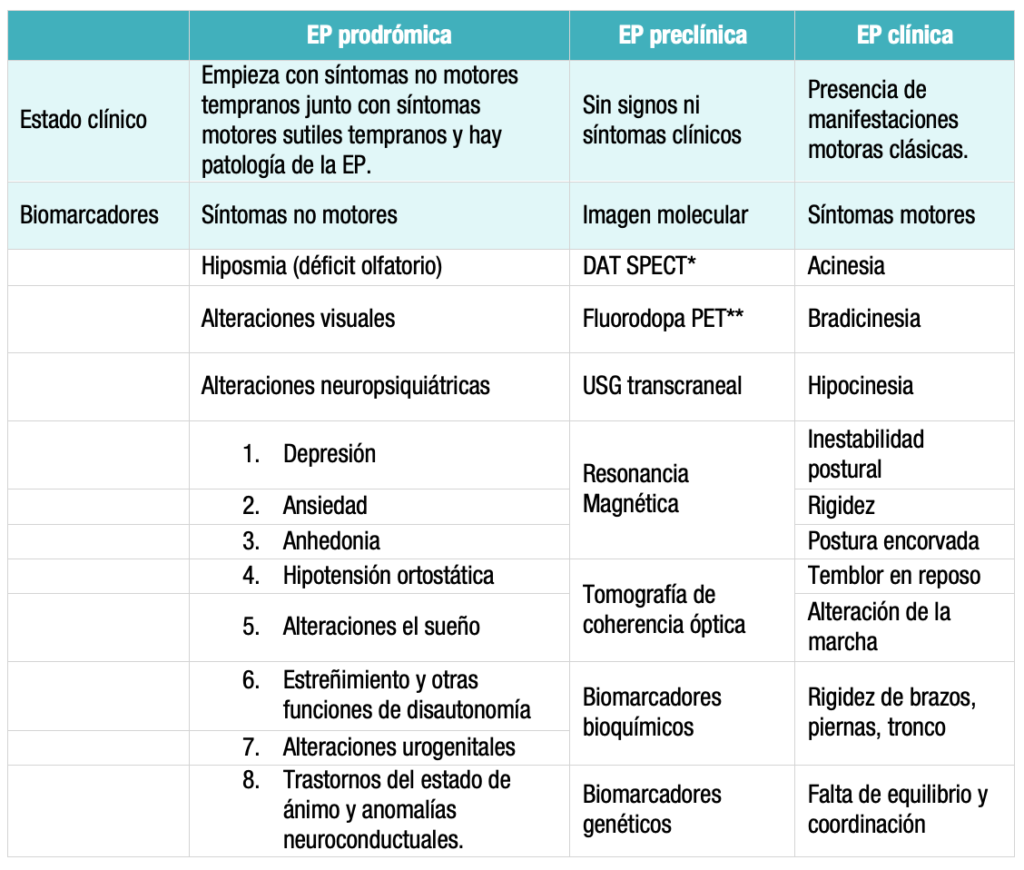 S. Lotankar et al.: Biomarkers for Parkinson’s Disease
S. Lotankar et al.: Biomarkers for Parkinson’s Disease
*Tomografía computarizada por emisión de fotón único con transportador de dopamina (DAT-SPECT)
**Tomografía por emisión de positrones con fluorodopa (F-DOPA-PET)
¿Existe alguna diferencia entre hombres y mujeres en la EP?
La gran mayoría de los casos de EP ocurren esporádicamente, solo el 10% de los pacientes portan mutaciones genéticas causantes de la enfermedad.6
Junto con el envejecimiento, la genética, el medio ambiente y el estado inmunológico, el papel del sexo biológico como factor importante en el desarrollo de la EP se ha debatido ampliamente en la última década. Existen claras diferencias relacionadas con el sexo en las características epidemiológicas y clínicas de la enfermedad: la EP afecta a los hombres dos veces más que a las mujeres, pero las mujeres tienen una tasa de mortalidad más alta y una progresión más rápida de la enfermedad.6
Según un metaanálisis reciente, se observa una incidencia creciente de EP relacionada con la edad en ambos sexos, pero con un aumento más predominante en los hombres, 60-69 y 70-79 años. La prevalencia creciente de la EP en los hombres se informa tanto para la enfermedad con y sin demencia. También se han encontrado diferencias basadas en el sexo para los factores que influyen pronóstico de vida en la EP. Un estudio reciente, que utilizó métodos de supervivencia relativa, mostró que un diagnóstico de EP con demencia tiene un mayor impacto en esperanza de vida en mujeres que en hombres.6
Además de las diferencias entre mujeres y hombres en la prevalencia y el pronóstico de la EP, muchos estudios han informado diferencias relacionadas con el sexo en la clínica.6
Diferencias en la sintomatología de la EP y los factores de riesgo entre mujeres y hombres. Los pacientes en EP presentan un fenotipo clínico diferente según el sexo.
Las opciones de tratamiento para pacientes con EP incluyen medidas no farmacológicas, farmacoterapia y terapia quirúrgica.7
El descubrimiento del déficit dopaminérgico en pacientes con EP condujo a intentos farmacológicos para restaurar la actividad dopaminérgica utilizando levodopa (L-DOPA, L-3,4 dihidroxifenilalanina) y agonistas del receptor de dopamina; estos fármacos benefician muchas de las características motoras del trastorno. Un enfoque alternativo y complementario ha sido restablecer el equilibrio entre las entradas colinérgicas y dopaminérgicas en los ganglios basales mediante el empleo de fármacos anticolinérgicos. La levodopa, un precursor de la dopamina, sigue siendo el agente más eficaz en el tratamiento de la enfermedad de Parkinson.7
La levodopa se administra con carbidopa, un inhibidor de la descarboxilasa periférica que bloquea la conversión periférica de levodopa en dopamina, lo que permite reducir la dosis y también minimizar sus efectos adversos periféricos.7
Los principales efectos adversos del tratamiento con levodopa son náuseas, complicaciones motoras que incluyen el fenómeno de “on – off”, discinesias y efectos intermitentes, confusión, alucinaciones, hipotensión ortostática y alteraciones del sueño.7
La apomorfina, otro agonista de la dopamina, se usa principalmente como terapia de rescate para el alivio temporal de los períodos inactivos de acinesia en pacientes con respuesta fluctuante a la terapia dopaminérgica. La monoaminooxidasa B selectiva (MAO-B) como la selegilina y la rasagilina retardan la descomposición de la dopamina en el cuerpo estriado, lo que beneficia a los pacientes con EP.7
La eficacia de estos agentes es modesta y se pueden utilizar como monoterapia en la EP inicial (Teoand Ho, 2013). Además, estos agentes se pueden utilizar como complementos para reducir los periodos “off” en pacientes con una respuesta en declive a la levodopa.7
La apomorfina subcutánea ha desempeñado un papel valioso en el tratamiento de los síntomas motores de la EP durante varias décadas y sigue siendo una terapia valiosa en la actualidad.
Schwab y sus colegas informaron por primera vez del efecto beneficioso del clorhidrato de apomorfina sobre el temblor y la rigidez en pacientes con EP. El uso exitoso de apomorfina subcutánea en combinación con domperidona fue confirmado en estudios posteriores de Corsini et al. y Hardie et al. En 1988, estudios fundamentales de Stibe et al. y Chaudhuri et al. informaron de la eficacia de la infusión subcutánea continua de apomorfina en el manejo de oscilaciones “on-off” refractarias en la EP
Referencias:
Palacios-Sánchez, Leonardo, Torres Nupan, Martha, & Botero-Meneses, Juan SebastiánJames, Parkinson and his essay on “shaking palsy”, two hundred years later. Arquivos de Neuro-Psiquiatria, 75(9), 671-672, 2017.
Reich, Stephen G.; Savitt, Joseph M, Parkinson Disease. Medical Clinics of North America, (), S002571251830138X–,
Samii A, Nutt JG, Ransom BR. Parkinson’s disease. Lancet. 2004 May 29;363(9423):1783-93.
Postuma, Ronald B.; Berg, Daniela; Stern, Matthew; Poewe, Werner; Olanow, C. Warren; Oertel, Wolfgang; Obeso, José; Marek, Kenneth; Litvan, Irene; Lang, Anthony E.; Halliday, Glenda; Goetz, Christopher G.; Gasser, Thomas; Dubois, Bruno; Chan, Piu; Bloem, Bastiaan R.; Adler, Charles H.; Deuschl, Günther. MDS clinical diagnostic criteria for Parkinson’s disease. Movement Disorders, 30(12), 1591–1601, 2015.
Lotankar, Sharvari; Prabhavalkar, Kedar S; Bhatt, Lokesh K, Biomarkers for Parkinson’s Disease: Recent Advancement. Neuroscience Bulletin, (), –.
Cerri, Silvia; Mus, Liudmila; Blandini, Fabio, Parkinson’s Disease in Women and Men: What’s the Difference?. Journal of Parkinson’s Disease, (), 1–15,
Kakkar, A.K., Dahiya, N., Management of Parkinson’s disease: Current and future pharmacotherapy. Eur J Pharmacol (2015)
Rosa-Grilo M, Qamar MA, Evans A, Chaudhuri KR. The efficacy of apomorphine – A non-motor perspective. Parkinsonism Relat Disord. 2016 Dec;33 Suppl 1:S28-S35.